
|
|||
|---|---|---|---|
|
|
Bioética: pesquisa em seres humanos e comitês de ética em pesquisa. Breves esclarecimentos |
|
|
|
*Prof. Educação Física Hospitalar da Rede Sarah de Hospitais do Aparelho Locomotor - Sarah Centro. Doutoranda em Ciências da Saúde pela UnB. **Médico Gastroenterologista do Hospital Universitário de Brasília Mestrando em Ciências da Saúde pela UnB |
Ana Cláudia Raposo Melo anamelo@linkexpress.com.br Vinícius Machado de Lima viniciusbsb@brturbo.com (Brasil) |
|
|
|
|
|||
|
|
http://www.efdeportes.com/ Revista Digital - Buenos Aires - Año 10 - N° 78 - Noviembre de 2004 |
|
|
1 / 1
1. IntroduçãoA realização de pesquisas por profissionais da área de saúde, em especial os profissionais de educação física, envolve em grande parte seres humanos, tornando necessária a avaliação dos projetos de pesquisa antes da sua fase de execução, objetivando avaliar, do ponto de vista ético, garantindo aos participantes da pesquisa integridade e dignidade.
Para tal, três princípios básicos são usados como norteadores: a beneficência, o respeito à pessoa e a justiça. Na área de saúde, esta avaliação está baseada na qualificação da equipe que desenvolverá o projeto, bem como no próprio projeto; na avaliação do risco-benefício; na utilização do consentimento livre e esclarecido e na avaliação e aprovação anterior à execução do projeto por um Comitê de Ética.
Porém a história da pesquisa envolvendo seres humanos percorreu caminhos perversos e duvidosos, apresentando episódios cercados de misticismo e crueldade. Apesar disto, houve momentos de lucidez e justiça humanitária, em que se tentou estabelecer padrões adequados para o estudo em humanos.
Em um estudo intitulado "An introduction in the study of experimental medicine", Claude Bernard (citado em Costa, 1999), tenta estabelecer parâmetros éticos para nortear o trabalho dos pesquisadores. Alguns anos mais tarde, em 1901, na Prússia, foi editada a Instrução sobre intervenções médicas com objetivos outros que não diagnóstico, terapêutica ou imunização, que proibia a realização de intervenções caso o paciente fosse menor ou não fosse totalmente competente em sua capacidade de fornecer o consentimento e/ou se este consentimento fosse fornecido sem informações adequadas sobre a pesquisa.
Por mais absurdo que possa parecer, no ano de 1931, o Governo Alemão possuía um detalhado regulamento sobre procedimentos terapêuticos diferenciados de experimentação humana, sendo este estabelecido pelo Ministério do Interior Germânico. Visava coibir o abuso e o desrespeito à dignidade humana nas pesquisas. Fato que não se verificou durante a Segunda Guerra Mundial, período durante o qual surgiram pesquisas envolvendo seres humanos na Alemanha Nazista, que ultrapassaram todos os limites de responsabilidade. Com a divulgação das atrocidades envolvendo médicos e pesquisadores alemães, a comunidade mundial organizou-se para julgá-los, como criminosos de guerra, no Tribunal de Nuremberg em 1947.
Em conseqüência do julgamento de Nuremberg, a pesquisa médica envolvendo seres humanos teve um marco deontológico no ano de 1947, que foi o surgimento do Código de Nuremberg. Este, em linhas gerais, abrangia temas como o consentimento voluntário, informações essenciais para os sujeitos da pesquisa e a não indução à participação. Determinava que a experiência tivesse que apresentar resultados vantajosos não alcançáveis por outros métodos e exigia a realização da experimentação em animais anteriormente à pesquisa em humanos. O sofrimento deveria ser evitado, o risco minimizado e, na possibilidade de morte, o projeto não deveria ser realizado.
Porém apesar do conhecimento dos horrores acontecidos nos campos de concentração e da elaboração do Código de Nuremberg, a realização de pesquisas com seres humanos que feriam os princípios éticos fundamentais continuou a ser realizadas.
No ano de 1966, foi criado um novo documento pela Associação Médica Mundial, conhecido como Declaração de Helsinque. Foi dividida em: princípios básicos, pesquisa médica combinada com cuidados profissionais e pesquisa biomédica não-terapêutica envolvendo seres humanos. Estes abordam em bases mínimas necessárias à realização de pesquisas envolvendo seres humanos. A Declaração de Helsinque, em linhas gerais, trata da necessidade de obediência a princípios científicos aceitos, bem como, da revisão ética e científica e boa qualificação dos pesquisadores. Manteve a necessidade de consentimento e fornecimento de informações essenciais para o sujeito, avaliação dos riscos/benefícios, assegurando aos participantes dos estudos os melhores métodos diagnósticos e terapêuticos existentes após término da pesquisa. Também, condena o uso do placebo quando já existe tratamento eficaz estabelecido.
Porém apesar da existência do Código de Nuremberg e da Declaração de Helsinque, muitas pesquisas ainda continuaram a ser realizadas cometendo atrocidades em seres humanos. Este fato foi denunciado por Henrry K. Beecher em 1966, através de um artigo publicado, onde analisou 22 pesquisas em que ocorriam maus-tratos a seres humanos. Com estas denúncias, cresceu a preocupação com a "proteção" dos direitos dos sujeitos da pesquisa.
A Declaração de Helsinque sofreu algumas revisões durante as Assembléias Médicas Mundiais, sendo a primeira realizada no Japão no ano de 1975, seguida pela revisão na Itália em 1983, Hong Kong em 1989, África do Sul em 1996 e, por último, na Escócia no ano de 2000.
O Conselho para Organizações Internacionais de Ciências Médicas (CIOMS) e a Organização Mundial de Saúde (OMS), objetivando nortear, do ponto de vista ético, a condução de pesquisas envolvendo seres humanos, de acordo com os princípios enunciados pela Declaração de Helsinque, publicou no ano de 1993 as Diretrizes Éticas Internacionais para Pesquisas Biomédicas Envolvendo Seres Humanos, abordando temas como a necessidade de consentimento pós-esclarecimento individual, com informações essenciais para os sujeitos; a não indução à participação; regras para pesquisa envolvendo: crianças, portadores de distúrbios mentais, prisioneiros, comunidades subdesenvolvidas, gestantes nutrizes. Abordou, também, a necessidade de consentimento da comunidade em estudos epidemiológicos, avaliação risco/benefício em todo tipo de pesquisa envolvendo seres humanos, sigilo dos dados obtidos, compensação por danos, revisão ética e cientifica e as obrigações dos países no desenvolvimento da pesquisa.
No Brasil, a regulamentação das pesquisas envolvendo seres humanos teve seu marco inicial com a Resolução N° 01 do Conselho Nacional de Saúde (CNS) no ano de 1988 (CNS - Resolução 01/88). Esta normatizou os aspectos éticos da pesquisa em seres humanos; a pesquisa de novos recursos profiláticos, diagnósticos, terapêuticos e de reabilitação; a pesquisa com menores de idade, mulheres e sujeitos; a pesquisa realizada em órgãos, tecidos e seus derivados; a pesquisa em farmacologia e pesquisas diversas. Regulamentou, também, o credenciamento de centros de pesquisas no país e recomendou a criação de comitês internos nas instituições de saúde. A aceitação desta resolução foi inexpressiva e sua aplicação prática foi considerada insatisfatória, tendo, contudo, o mérito de ser a tentativa inicial de normatização nacional das pesquisas em seres humanos.
Estando o Brasil inserido no Tratado do Mercado Comum do Sul, o Mercosul, foi elaborada a Resolução N° 129/96, intitulada de Boas Práticas Clínicas - Grupo Mercado Comum (MERCOSUL), abordando a Pesquisa em Farmacologia Clínica nos aspectos de autorização, acompanhamento, responsabilidades dos pesquisadores e dos patrocinadores, requisitos éticos e a necessidade de obtenção de informação pré-clínica e clínica.
2. Resolução 196/96Com a crescente discussão ética mundial, e após o insucesso da tentativa inicial de normatização com a Resolução 01/88, surgiu a necessidade de um novo documento nacional abordando os aspectos éticos em pesquisa. Deste modo foi criada a Resolução 196/96 do Conselho Nacional de Saúde. Em 9 de outubro de 1996, o Ministro da Saúde Adib Jatene assinou esta resolução em que constam as Diretrizes e Normas Regulamentadoras de Pesquisa Envolvendo Seres Humanos. Este documento foi elaborado após discussão entre sociedade civil organizada, comunidade científica, sujeitos de pesquisa e Estado, tendo como base os seguintes documentos internacionais:
Código de Nuremberg (1947)
Declaração dos Direitos do Homem (1948)
Declaração de Helsinque (1964)
Acordo Internacional sobre Direitos Civis e Políticos (1966)
Propostas de Diretrizes Éticas Internacionais para Pesquisas Biomédicas Envolvendo Seres Humanos (1982)
Têm como objetivo maior assegurar os direitos e deveres da comunidade científica, Estado e, com especial preocupação, dos sujeitos da pesquisa. Para tal, já no seu preâmbulo, fica bem clara a incorporação dos princípios de autonomia, não-maleficência, beneficência e justiça, que são os quatro referenciais básicos da bioética. É, também, colocado o caráter contextual desta resolução, o que implica em necessidade de constante revisão já que há permanente evolução técnico-científica e ética.
Alguns termos e definições constam no documento e são úteis para seu entendimento, a saber:
Pesquisa: atividade com objetivo de desenvolver ou contribuir para o conhecimento generalizável.
Pesquisa em seres humanos: pesquisa que individual ou coletivamente, direta ou indiretamente, parcial ou totalmente, envolva o ser humano.
Pesquisador responsável: responsável pela coordenação e realização da pesquisa e integridade e bem estar do sujeito da pesquisa.
Risco da pesquisa: possibilidade de dano físico, psíquico, moral, intelectual, social, cultural ou espiritual do ser humano na pesquisa ou dela decorrente.
Sujeito da pesquisa: é o pesquisado, de caráter voluntário, sendo vedada qualquer forma de remuneração.
Consentimento livre e esclarecido: anuência do sujeito livre de fraude, simulação ou erro, dependência, subordinação ou intimidação, após explicação pormenorizada de todos os aspectos da pesquisa, incluindo riscos e incômodos, elaborada em um termo, autorizando sua participação voluntária.
Indenização: cobertura material em reparação a dano causado pela pesquisa.
Ressarcimento: cobertura das despesas decorrentes da pesquisa
Comitês de Ética em Pesquisa - CEP: colegiados interdisciplinares e independentes, de caráter consultivo, deliberativo e educativo, com objetivo de defender os interesses dos sujeitos da pesquisa em sua integridade e dignidade e contribuir para o desenvolvimento da pesquisa dentro de padrões éticos.
Vulnerável: pessoa cuja capacidade de autodeterminação esteja reduzida, sobretudo para o consentimento livre e esclarecido.
Incapacidade: falta de capacidade civil do sujeito da pesquisa para o consentimento.
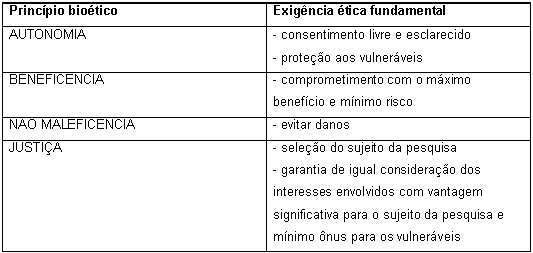
2.1. Aspectos éticos da pesquisa envolvendo seres humanosPara que determinada pesquisa seja aceitável, certas exigências éticas fundamentais e científicas devem ser respeitadas. Algumas destas são fortemente baseadas nos princípios básicos da Bioética e estão listadas no quadro abaixo:
Será considerada pesquisa e estará submetida à Resolução 196/96 todo procedimento em seres humanos, seja de que natureza for, de aceitação ainda não consagrada cientificamente. Estas pesquisas deverão atender aos seguintes quesitos:
ser justificada cientificamente / ter possibilidade concreta de responder as incertezas.
ter fundamentação científica prévia (Ex: intervenção - fase pré-clínica)
ser a único modo de se obter determinado conhecimento.
os benefícios devem superar riscos
obedecer à metodologia adequada. Assegurar numa distribuição aleatória que não seja possível estabelecer vantagem de um procedimento sobre outro.
justificar placebo (sua necessidade metodológica) (considerar primordialmente a não-maleficência - se tratamento consagrado já existe, o placebo é injustificável).
obter consentimento livre e esclarecido
garantir recursos humanos e materiais para o bem estar do sujeito da pesquisa
garantir privacidade e confidencialidade, assegurando a não utilização das informações em prejuízo das pessoas.
envolver sempre que possível indivíduos com autonomia plena, evitando vulneráveis a menos que a investigação traga benefício direto a estes.
respeitar valores culturais, sociais, morais, religiosos, éticos e hábitos e costumes em pesquisa com comunidades.
comunicar os resultados às autoridades sanitárias sempre que puderem contribuir para melhoria da condições de saúde comunitária, preservando a imagem do sujeito da pesquisa (evitar estigmatização).
assegurar ao sujeito da pesquisa os benefícios resultantes do projeto (retorno social, acesso aos procedimentos, produtos ou agentes da pesquisa).
comprovar as vantagens para sujeitos de pesquisa e para o Brasil em pesquisas conduzida do exterior. Deve possuir instituição e pesquisador nacionais co-responsáveis. Deve incluir aprovação no país de origem. Deve ser aprovado por comitê de ética em pesquisa nacional
utilizar o material biológico e dados exclusivamente para finalidade prevista.
levar em conta, nas pesquisas com mulheres grávidas ou em idade fértil, as conseqüências na fertilidade, gravidez e amamentação.
descontinuar o estudo somente após análise das razões pelo comitê que o aprovou.
2.2. Consentimento livre e esclarecidoO consentimento livre e esclarecido consiste em instrumento para se tentar assegurar a autonomia do sujeito da pesquisa, através da obtenção da sua anuência à participação. Seu correto uso pressupõe a concordância, sem qualquer coerção, após fornecimento e compreensão da informação sobre os procedimentos. Tem como objetivo principal a proteção destes indivíduos, não sendo, como o consentimento informado usado no passado, um instrumento de defesa do pesquisador e instituição diante de conseqüências negativas da pesquisa. Não é infalível, principalmente em um país como o nosso em que a grande maioria dos sujeitos de pesquisa é extremante vulnerável por suas condições sociais, culturais e econômicas desiguais. Apesar disto, foi um grande avanço e tem sido útil se utilizado da forma correta. Para tal é necessário que seja elaborado em linguagem acessível e possua informações sobre:
Justificativa, objetivo e procedimentos (porque, para que e como).
Desconfortos, riscos e benefícios.
Identificação do responsável, forma de acompanhamento e assistência.
Garantia de esclarecimentos a qualquer momento e informação clara sobre grupo controle e placebo.
Liberdade para retirar-se sem penalização
Privacidade de sujeito da pesquisa / confidencialidade.
Formas de ressarcimento.
Formas de indenização.
Não são permitidas ressalvas que impliquem isenção das responsabilidades do pesquisador e instituição. Além disto, todo consentimento deve ser aprovado pelo Comitê de Ética e conter a assinatura do sujeito da pesquisa. Uma via deve permanecer com este e outra com o pesquisador.
Um cuidado especial deve ser dispensado às situações de restrição à liberdade ou limitação ao esclarecimento do consentimento. Nas pesquisas com crianças, adolescentes, portadores de doença mental e outros sujeitos com substancial redução de sua capacidade de consentimento, deve haver:
Justificativa bem fundamentada para escolha de um destes grupos.
Aprovação pelo Comitê de Ética.
Consentimento livre e esclarecido do representante legal.
Informação para o indivíduo no limite de sua capacidade.
Sujeitos expostos a condicionamentos específicos ou influência de autoridade (estudantes, militares, empregados, presidiários, asilos, associações religiosas) devem ter garantia de plena liberdade de consentimento. Em comunidades culturalmente diferenciadas como as indígenas, o consentimento deve ser individual e comunitário através dos seus líderes.
2.3. Riscos e benefíciosA presença de risco é uma característica inerente às pesquisas em seres humanos. Este risco pode ser individual, coletivo, imediato, tardio, físico, psíquico, dentre outros, contudo sempre existirá em menor ou maior grau. Assim sendo, é aceitável quando a finalidade de determinada pesquisa justificá-lo, da seguinte forma:
Se a pesquisa oferecer elevada possibilidade de entendimento, prevenção ou alívio do problema que afeta o sujeito.
Se for de grande importância o benefício esperado.
Se o benefício for igual ou maior que aquele de outra alternativa já estabelecida.
Caso um dano ou risco não identificado surja em determinada pesquisa, não tendo sido previsto no termo de consentimento, o estudo deve ser interrompido. Da mesma forma, tão logo seja constatada a superioridade de um método sobre outro, o melhor regime deverá ser oferecido a todos os sujeitos. Este tópico foi alvo de grande discussão durante a revisão da Declaração de Helsinque na Assembléia Geral da Associação Médica Mundial em outubro de 2000. Há uma tentativa de mudança no sentido de não mais se oferecer o melhor regime existente, mas sim, o melhor regime disponível no local em que a pesquisa é realizada.
Afirmações como estas abrem, inclusive, uma brecha para o uso do placebo mesmo quando já houver um tratamento eficaz. Esta proposta, denominada duplo-standard, vem sendo defendida pela poderosa indústria farmacêutica, que, com sua aprovação, reduziria enormemente os custos de desenvolvimento de medicamentos, principalmente em pesquisas nos países mais pobres, porém com prejuízo enorme para os sujeitos da pesquisa. Esta modificação não foi aprovada, mas permaneceu em aberto para nova discussão na próxima revisão da Declaração de Helsinque.
Ainda com relação aos danos sofridos pelos sujeitos da pesquisa, é importante ressaltar que, previstos ou não, se ocorrerem, são de responsabilidade do pesquisador e instituição. Neste caso, os sujeitos devem receber assistência integral, tendo direito a uma indenização.
2.4. Protocolo de pesquisaTodo protocolo deve apresentar os dados do pesquisador, instituição e da pesquisa, além da fundamentação científica que a justifique, com análise crítica dos riscos e benefícios. O pesquisador deve assumir, também, o compromisso de cumprir a Resolução 196/96 e de tornar os resultados de sua pesquisa públicos, mesmo que sejam desfavoráveis.
2.5. Comitês de ética em pesquisa (CEP)Com a Resolução 196/96 surgiram os Comitês de Ética em Pesquisa (CEP) institucionais, multidisciplinares na sua composição, com a função de analisar as pesquisas em seres humanos nas diversas áreas de conhecimento, bem como fomentar discussão sobre bioética.
Segundo o documento das diretrizes e normas, toda instituição deveria criar, organizar e manter um CEP e toda pesquisa envolvendo seres humanos deveria ser submetida à aprovação desse comitê. Cada CEP deve ser composto por no mínimo sete membros não remunerados, incluindo profissionais da saúde, ciências exatas, sociais, humanas e, pelo menos, um representante dos usuários da instituição, possuindo, assim, caráter multi e transdisciplinar. A metade destes membros é escolhida pela instituição e o restante por eleição entre aqueles com experiência em pesquisa, com mandato de três anos.
Ao não permitir que mais da metade dos integrantes de um CEP seja formada por apenas uma categoria profissional, a resolução impede uma composição corporativista. Do mesmo modo, os dois sexos devem estar representados de maneira semelhante, não sendo permitido membro envolvido com a pesquisa analisada.
São atribuições dos CEP:
Revisar os protocolos de pesquisa, resguardando a integridade e direito dos voluntários.
Emitir parecer enquadrando o protocolo em: aprovado, com pendência (60 dias), retirado, não aprovado, aprovado em encaminhado ao CONEP nos casos relativos às ÁREAS TEMÁTICAS ESPECIAIS (discutidas abaixo).
Acompanhar o desenvolvimento do projeto.
Ser consultivo e educativo, fomentando a reflexão sobre ética na ciência.
Receber denúncia e decidir o destino da pesquisa.
A interrupção de uma pesquisa sem justificativa aceita pelo CEP é considerada conduta não ética.
2.6. Comissão nacional de ética em pesquisa (CONEP)É a instância superior aos CEP, vinculada ao Conselho Nacional de Saúde (CNS), de natureza consultiva, deliberativa, normativa, educativa e independente. Também composta de forma multi e transdisciplinar por 13 membros sendo cinco personalidades destacadas no campo da ética e saúde e oito personalidades de atuação outras áreas.
Dentre suas atribuições estão:
Examinar os aspectos éticos das pesquisas em seres humanos.
Adequar e atualizar as normas destas pesquisas.
Estimular a criação dos CEP.
Instância final de recursos.
Rever responsabilidade e interromper pesquisas.
Constituir sistema de informação e acompanhar, do ponto de vista ético, as pesquisas.
Divulgar estas normas.
Estabelecer normas para credenciamento dos centros de pesquisa.
Analisar todo projeto encaminhado pelos CEP para parecer.
Aprovar e acompanhar protocolos de pesquisa nas ÁREAS TEMÁTICAS ESPECIAIS.
2.6.1. Áreas temáticas especiais
Genética humanaOs pareceres do CONEP relativos à área de Genética Humana são baseados, no que se refere aos aspectos específicos, nas Instruções Normativas nº8 e 9 da Comissão Técnica Nacional de Biossegurança (CTNBio). Estas instruções reafirmam os princípios da Resolução 196/96, dispondo sobre manipulação genética e clonagem de seres humanos, com as seguintes normas:
São vedadas, em seres humanos, quaisquer atividades de manipulação do genoma humano que envolva células responsáveis pela formação dos gametas (células germinativas), bem como, células com capacidade para formar células germinais ou diferenciar-se em um indivíduo (células tronco).
Não é permitida a clonagem de um ser humano a partir de uma célula (clonagem radical).
Dentro desta área são passíveis de aprovação apenas projetos que envolvam manipulação genética de células somáticas.
Reprodução humanaCom objetivo de complementar as Diretrizes de Normas Regulamentadoras de Pesquisa Envolvendo Seres Humanos, o Conselho Nacional de Saúde, aprovou a Resolução 303/00, relativa à área de reprodução humana. Nesta fica definido que os sujeitos da pesquisa serão todos aqueles afetados pelos procedimentos estudados. Estabelece também, que dentro desta área temática, todas as pesquisas com intervenção em reprodução assistida; anticoncepção; manipulação de gametas, pré-embriões, embriões e feto e medicina fetal, devem ser, após parecer do CEP, obrigatoriamente encaminhadas para avaliação do CONEP.
Fármacos, vacinas e testes diagnósticos.A Resolução 251/97 que incorpora a Resolução 196/96 e reporta-se à Resolução de Grupo Mercado Comum (GMC) nº129/96, trata da normatização desta área temática. Nela é definida como pesquisa com novos fármacos, medicamentos, vacinas ou testes diagnósticos, todos os estudos com estes produtos em fase I, II, III e, ainda, fase IV quando abordar aplicação diferente daquela já estabelecida. Estas fases, definidas na Resolução do GMC, são:
Fase I - pesquisa em pequeno grupo voluntário visando avaliação inicial de segurança, farmacocinética e farmacodinâmica.
Fase II - estudo terapêutico piloto para se estabelecer segurança e relações dose-resposta.
Fase III - estudo terapêutico ampliado (ensaio clínico randomizado) explorando a relação risco-benefício e valor terapêutico relativo.
Fase IV - pesquisa pós-comercialização do produto, a fim de, na grande população, estabelecer-se o valor terapêutico e novas reações adversas.
Esta resolução apresenta aspectos de fundamental importância relativos aos direitos e proteção do sujeito da pesquisa. Nela consta que deve ser assegurado aos sujeitos da pesquisa, por parte do patrocinador, instituição e pesquisador, o acesso, após a comprovação, ao melhor procedimento diagnóstico ou terapêutico, inclusive àqueles do grupo controle quando houver. É, também, contrária ao uso de placebo quando um método terapêutico eficaz já existir. Estes dois aspectos, como já mencionado anteriormente, têm sido questionados nas revisões da Declaração de Helsinque. Sua modificação, por pressão da indústria farmacêutica, seria um imenso retrocesso na qualidade da regulamentação. A preocupação com este assunto levou o Brasil, previamente à revisão da Declaração de Helsinque de outubro de 2000, à homologação da Resolução CNS 301/00, que reforça as normas já estabelecidas, posicionando-se contrariamente às mudanças propostas.
Populações indígenasA preocupação com a vulnerabilidade do índio e de sua cultura e o interesse crescente em pesquisas com populações indígenas, muitas delas isoladas, fez com que esta área obtivesse tratamento especial, com resolução complementar (Resolução N° 304/00). Esta coloca de forma bem clara a necessidade de que a pesquisa respeite os aspectos culturais peculiares, não admitindo exploração das comunidades indígenas. Outras exigências da resolução são:
Deve ser obtida a anuência coletiva, além do consentimento individual.
A igualdade de consideração de interesses deve ser respeitada.
Comunidades isoladas devem ser evitadas.
Não são aceitos patenteamentos de produtos obtidos em pesquisas com indígenas.
Para estes efeitos, são índios todos aqueles que se considerarem pertencentes a uma comunidade indígena e forem por ela aceitos como tais.
Pesquisas coordenadas do exterior ou com participação estrangeiraOs países em desenvolvimento têm se tornado, cada vez mais, local de pesquisa dos grandes laboratórios multinacionais. A Resolução N° 292/99 foi criada visando regulamentar esta prática. Nela é colocada a necessidade de que o ônus e benefícios sejam distribuídos de forma justa entre as partes envolvidas. Fica, também, estabelecida a obrigatoriedade da aprovação da pesquisa pelo comitê de ética do país de origem e, se não desenvolvida nesse país, a razão para tal de ser apresentada ao CONEP para análise.
Equipamentos, insumos e dispositivos para saúde novos ou não registrados no país
Novos procedimentos não consagrados na literatura
Projetos que envolvam aspectos de biossegurança
3. Considerações finaisOs documentos como a Declaração de Helsinque e as Diretrizes e Normas Regulamentadoras de Pesquisa Envolvendo Seres Humanos (Resolução 196/96) são importantes referências oficiais para os pesquisadores, apesar de alguns pesquisadores, inclusive da área de saúde/educação física negligenciarem ou até desconhecerem as normas para realização de uma pesquisa envolvendo seres humanos. Contudo, o maior impacto destes, com valorização dos Comitês de Ética em Pesquisa, só ocorreu com a exigência para publicação, por parte das revistas científicas nacionais e internacionais, de aprovação ética prévia da pesquisa por um comitê institucional.
A necessidade do cumprimento destas resoluções tem uma razão muito maior que somente o enquadramento da pesquisa em regras de publicação. O objetivo primordial das diretrizes e normas é a proteção do ser humano na sua integridade e dignidade, fazendo com que o desenvolvimento científico ocorra de forma ética. Nesse caminho, os CEP e o CONEP são instrumentos fundamentais, multi e transdisciplinares, e, portanto pluralistas, capazes de uma avaliação adequada dos protocolos de pesquisa antes da sua execução, impedindo assim a ocorrência de transgressões éticas de conseqüências eventualmente graves, principalmente para a parte mais frágil, o sujeito da pesquisa.
Se ampliarmos o conceito de vulnerabilidade, incluindo não só aqueles em situações específicas de redução da autonomia, como crianças e prisioneiros, mas sim, todos que vivem em condições de desigualdade, seja social, econômica, cultural, política, étnica e educacional, teremos como vulnerável a quase totalidade dos sujeitos da pesquisa no Brasil. Deste modo é fundamental que muitas destas resoluções sejam fortalecidas, tornando-se leis, e que a rede de CEP seja constantemente avaliada, treinada e ampliada.
Os CEP e CONEP devem se manter atuantes, fomentando a discussão sobre bioética, reavaliando e adequando as diretrizes e normas à evolução técnico-científica e social. A proteção ao nosso sujeito da pesquisa, extremamente vulnerável, deve ser ampliada com a correção de distorções resultantes de uma regulamentação adaptada de normas estrangeiras, moldadas em um princípio de autonomia excessiva, inadequado frente às condições do povo brasileiro.
Referências bibliográficas
Brasil - Ministério da Saúde. Diretrizes e Normas Regulamentadoras de Pesquisa Envolvendo Seres Humanos. Resolução 196/96 do Conselho Nacional de Saúde, 1996, 19 p.
CIOMS/OMS. Diretrizes Éticas Internacionais para Pesquisas Biomédicas Envolvendo Seres Humanos (incluindo Declaração de Helsinque corrigida, 1989 e As Fases dos Testes Clínicos de Vacinas e Medicamentos). Bioética (CFM) 3(2);95-131, 1995.
Costa, SIF. Ética e pesquisa clínica segundo Henry Beecher. O Mundo da Saúde, 23(5):336-341, 1999.
Garrafa, V & do Prado, MM. Tentativas de modificações na Declaração de Helsinki: fundamentalismo econômico, imperialismo ético e controle social (Brasília, UnB, Série Bioética Nº 08, 2000).
Guimarães, MCS & Novaes SC. Vulneráveis. Instituto de Medicina Tropical. Faculdade de Medicina. USP. Disponível em: http://www.bioetica.ufrgs.br/bioetica.htm
Pareceres, resoluções, diretrizes, declarações, leis e projetos relacionados à Bioética. CREMESP/CFM. Disponível em: http://www.bioetica.org.br/legislacao
Pesquisas Coordenadas do Exterior ou com Participação Estrangeira. Resolução 292/99 do Conselho Nacional de Saúde. Unimep. Disponível em: http://www.unimep.br/cepesquisa/resolucoes/resolucaoCNS292-99.htm
Resoluções do Conselho Nacional de Saúde. Núcleo de Ética Aplicada e Bioética/ Escola Nacional de Saúde Pública/FIOCRUZ. Disponível em: http://www.ensp.fiocruz.br/etica/Arq/resolu.htm
| |
|
|---|---|
|
revista
digital · Año 10 · N° 78 | Buenos Aires, Noviembre 2004 |
|