Introdução
A miocardiopatia periparto (MCP) é uma entidade rara, de etiologia idiopática.
Sua definição inclui 4 critérios, descritos por Demakis em 1971 e revisados
em 2010 pela Heart Failure Association of the European Society of Cardiology
Working Group, sendo eles: 1) desenvolvimento de insuficiência cardíaca (IC)
no último mês de gestação ou até o quinto mês de puerpério; 2) ausência
de causa identificável para a IC; 3) ausência de cardiopatia conhecida antes
do último mês de gestação; 4) disfunção sistólica do ventrículo esquerdo
(VE) caracterizada por fração de ejeção (FE) menor que 45% ao
ecocardiograma, exame complementar padrão ouro para diagnóstico de IC. 1, 2
A causa da MCP permanece desconhecida, porém infecções virais e
participação de autoanticorpos tem sido implicadas na sua patogênese. Fatores
genéticos, resposta inadequada ao stress hemodinâmico da gestação,
ativação de citoquinas inflamatórias e tocólise prolongada também são
considerados. Quanto aos fatores de risco, idade materna avançada,
multiparidade, descendência africana, gravidez gemelar, hipertensão induzida
pela gravidez e uso de tocolíticos podem ser citados. Assim, a real causa
provavelmente é multifatorial. 3,4
Relata-se um caso de IC decorrente de MCP em paciente de 26 anos previamente
hígida.
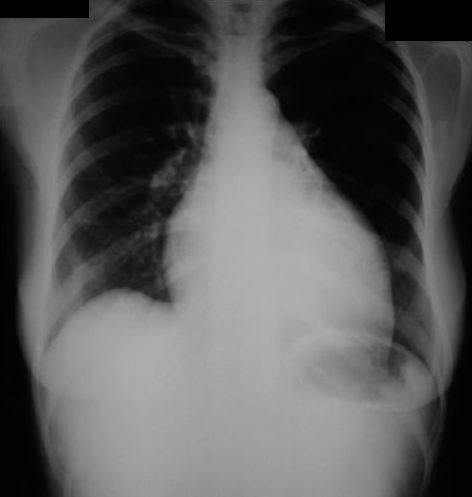
Figura
1. Radiografia do tórax em incidência póstero-anterior notando-se
retificação do arco médio e cardiomegalia
Relato
do caso
G.S.M, 26 anos, negra, G2P2A0, previamente hígida, foi admitida em unidade
hospitalar queixando-se de dor torácica, dispneia, taquicardia, náuseas e
vômitos, de início súbito. A paciente encontrava-se no 10º dia de puerpério
e relatava parto cesáreo a termo sem intercorrências, assim como
acompanhamento pré-natal dentro da normalidade. Ao exame verificou-se edema
importante de membros inferiores, crepitações em bases pulmonares, PA 90x70,
FC 120 bpm e SatO2 93%. Foi aventada como diagnóstico a MCP, solicitando-se
revisão laboratorial, radiografia de tórax, ECG e ecodopplercardiograma. O
hemograma demonstrou hemácias de 4,0 milhões/mm³, hemoglobina de 12,5%,
hematócrito de 34%, 8.100 leucócitos/mm³ e 224.000 plaquetas/mm³. No que se
refere aos demais exames laboratoriais, verificou-se ureia de 24 mg∕dL,
creatinina de 0,9 mg/dL, eletrólitos dentro da normalidade e D-dímero
negativo. Na radiografia de tórax (Figura 1) observa-se aumento do índice
cardio-torácio (ICT) e congestão em bases pulmonares. O ECG (Figura 2) revelou
má progressão de R de V1 a V3, bem como sobrecarga de átrio esquerdo com
sinal de Morris positivo. Já o ecodopplercardiograma demonstrou miocardiopatia
dilatada com aumento importante de câmaras esquerdas; déficit sistólico
global importante do VE (Fração de Ejeção: 32%); insuficiência mitral
moderada por dilatação do anel valvar; insuficiência tricúspide discreta,
hipertensão pulmonar leve e disfunção diastólica do VE (grau I). A partir da
confirmação diagnóstica, utilizou-se Furosemida (20 mg 12/12h) e dobutamina
endovenosa, além de ter sido iniciada a profilaxia contra tromboembolismo
pulmonar (Clexane 40 mg/dia). Nos dias seguintes de internação foram ainda
associados carvedilol (3,125mg 12/12h) e espironolactona (25mg/dia), sendo que o
primeiro não foi bem tolerado pela paciente. Assim, procedeu-se com aumento da
dose da furosemida e inserção do captopril (12,5mg 12/12h). A paciente evoluiu
com melhora clínica dos sintomas e estabilidade hemodinâmica; tendo sido
reintroduzido betabloqueador (carvedilol 3,125mg) e aumentada a dose do inibidor
da ECA (captopril 12,5mg 8/8h), que evitam remodelamento cardíaco e melhoram a
sobrevida. A mesma recebeu alta hospitalar no 12º dia de internação e
orientação para acompanhamento ambulatorial com o serviço de cardiologia.
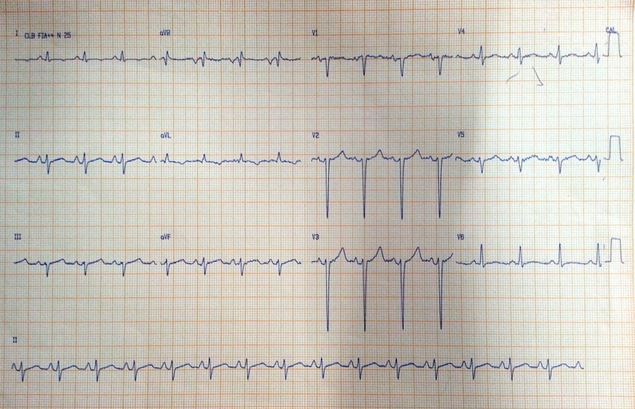
Figura
2. Má progressão de R de V1 a V3, bem como sobrecarga de átrio esquerdo
com sinal de Morris positivo
Discussão
A MCP é uma patologia infrequente que apresenta alta taxa de mortalidade,
sobretudo quando o diagnóstico e tratamento não são feitos prontamente. As
principais causas de óbito são insuficiência cardíaca, arritmias ou eventos
embólicos. A incidência mostra-se variável e depende da área geográfica em
estudo; no Brasil, ainda não há estimativa da real incidência. 3,5
Clinicamente, os sintomas apresentados são os clássicos da IC, como dispneia,
dispneia aos esforços, dispneia paroxística noturna, edema de membros
inferiores e fadiga; sendo comumente o quadro de apresentação da doença.
Porém, muitas vezes, esses sintomas são semelhantes àqueles presentes na
gestação avançada e no período pós-parto, tornando o diagnóstico
laborioso. Sendo assim, os sintomas são frequentemente atribuídos ao período
gestacional normal, sono irregular ou até mesmo um diagnóstico equivocado de
pneumonia. Porém, significativa parcela das pacientes apresentam sintomas
avançados de IC, NYHA (New York Heart Association) 3 ou 4, ao diagnóstico.
Casos menos severos e apresentações atípicas (eventos tromboembólicos
cerebrais, periféricos e mesentéricos) contribuem para a dificuldade
diagnóstica da MCP. 6, 7
A propedêutica é realizada através de ECG, radiografia de tórax e
ecodopplercardiograma; devendo este último ser repetido em caso de piora
clínica ou a cada 6 meses para acompanhar a recuperação, que pode estender-se
por até três anos. O ecocardiograma mostra frequentemente disfunção e
dilatação do ventrículo esquerdo. Já a ressonância magnética pode também
ser útil para identificar disfunção ventricular; além de detectar presença
de miocardite. Nesse caso, a biópsia endomiocárdica deve ser eventualmente
considerada. 3, 8
A biópsia endomiocárdica já foi mais utilizada para diagnóstico de
miocardite e indicação de terapia imunossupressora, sendo igualmente
recomendada em pacientes que não apresentam melhora com o tratamento
convencional, nas primeiras semanas após o diagnóstico. Recentemente, foi
demonstrado que a incidência de miocardite é relativamente baixa, não
diferindo muito da encontrada em mulheres com miocardiopatia dilatada
idiopática. Todavia, quando realizada, deve-se incluir o teste de PCR para
grande espectro viral antes do uso da terapia imunossupressora. O diagnóstico
da etiologia viral possibilita o uso de terapia antiviral específica.3
O tratamento dessa patologia geralmente segue a terapêutica clássica da IC,
atentando-se à contraindicação de inibidores da ECA e espironolactona durante
o período gestacional; que podem ser normalmente utilizadas durante a
lactação. Tais drogas são substituídas na gestação pela hidralazina,
associada ou não a nitratos. Outra vertente importante é a anticoagulação,
com heparina antes do parto e anticoagulante oral após e durante a
descompensação, visando à profilaxia de eventos tromboembólicos. Em casos
graves de IC, podem ser necessários os inotrópicos, como a dopamina,
dobutamina ou milrinone, bem como marca-passo e cardiodesfibrilador implantável
para estabilização hemodinâmica. 3, 9
A terapia imunossupressora deve ser restrita às pacientes com miocardite
linfocitária e ausência de partículas virais confirmada pela biópsia,
especialmente na ausência de melhora clínica após duas semanas de tratamento
clássico para IC. 3
No que se refere à via de parto, desde que haja condições para a sua
realização, a escolha é a vaginal. O prognóstico é pior em multíparas, com
idade superior a 30 anos e raça negra; mas futuras gestações devem ser
desaconselhadas em pacientes que permanecerem com disfunção ventricular após
a gravidez e puerpério1.
Referências
-
Patta
CB, Nunes RD. Miocardiopatia periparto: relato de caso. Arq. Catarin. Med.
2012; 41(3): 68-70.
-
Sliwa
K et al. Current state of knowledge on etiology, diagnosis,
management, and therapy of peripartum cardiomyopathy: a position statement
from the Heart Failure Association of the European Society of Cardiology
Working Group on peripartum cardiomyopathy. Eur J Heart Fail 2010;
12:767-78.
-
Tedoldi
CL. Diretriz da Sociedade Brasileira de Cardiologia para Gravidez na Mulher
Portadora de Cardiopatia. Arq Bras Cardiol 2009; 93(6 supl.1): e110-e178.
-
Huang
GY, Zhang LY, Long-Le MA, Le-Xin Wang. Clinical characteristics and risk
factors for peripartum cardiomyopathy. African Health Sciences Vol 12 No 1
March 2012.
-
Ardila
DFP, Hurtado SN, Osorio EMA, Rosero AA. Miocardiopatía periparto. Rev Insuf
Cardíaca 2009; 4 (4): 177-183.
-
Capriola
M. Peripartum cardiomyopathy: a review. International Journal of Women’s
Health 2013; 5: 1-8.
-
Shah
T, Ather S, Bavishi C, Bambhroliya A, Ma T, Bozkurt B. Peripartum
cardiomyopathy: a contemporary review. Methodist
Debakey Cardiovasc J. 2013 Jan-Mar; 9(1): 38–43.
-
Krejci
J et al. The variable clinical course of peripartum cardiomyopathy.
Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub. 2012; 156: XX.
-
Tay
ELW, Yip JWL, Poh KK. Peripartum cardiomyopathy: when labour turns to
heartbreak. Singapore Med J 2013; 54(1) : 1-2.
-
Urbanetz
AA, Carraro EA, Kalache LF, Kalache PF, Lobo PH, Germiniani H et al.
Cardiomiopatia periparto. FEMINA. 2009 Jan; 37(1): 13-18.
Outros artigos em
Portugués
 |
|
|
EFDeportes.com, Revista
Digital · Año 19 · N° 196 | Buenos Aires,
Septiembre de 2014
© 1997-2014 Derechos reservados
|



