
|
|||
|---|---|---|---|
|
|
Lesiones del ligamento cruzado anterior y la aplicación de factores de crecimiento para su tratamiento |
|
|
|
Centro Público de Estudios para la Enseñanza de los Deportes. Gobierno Vasco (España) |
Sergio Edeso Aritz Urdampilleta |
|
|
|
Resumen Las lesiones del ligamento cruzado anterior de la rodilla son comunes y producen discapacidad en personas jóvenes y deportistas; además, predisponen a lesiones posteriores de la rodilla y a osteoartritis temprana. Esta revisión actualiza los siguientes aspectos de importancia para la comprensión del tratamiento de estas lesiones, haciendo hincapié en la utilización de plasma autólogo rico en factores de crecimiento (PRGF) para ello. La utilización de plasma autólogo rico en factores de crecimiento (PRGF), tiene como objetivo mejorar la evolución quirúrgica, reforzando y potenciando el proceso de reparación fisiológica. Además permite una regeneración más rápida y de mayor calidad en los tejidos conjuntivos dañados, en este caso, en la cirugía artroscópica de las plastias del ligamento cruzado anterior. Cuando se utiliza PRGF asociado a la cirugía, las complicaciones postoperatorias y los signos inflamatorios son menores, se acelera la cicatrización de las heridas y la integración de la plastia. La utilización de PRGF a priori no implica ningún tipo riesgo ni complicación para el paciente, y los beneficios de su aplicación son considerables. Palabras clave: Ligamento cruzado anterior. Rodilla. Lesiones. Tratamiento. PRGF.
|
|||
|
|
EFDeportes.com, Revista Digital. Buenos Aires, Año 18, Nº 179, Abril de 2013. http://www.efdeportes.com/ |
|
|
1 / 1
Introducción
La historia natural y el tratamiento de las lesiones del ligamento cruzado anterior de la rodilla (LCA) generan mucha controversia, porque en algunos individuos la articulación queda poco funcional después de una ruptura del LCA, mientras que en otros permanece relativamente asintomática y el paciente es capaz de retomar una actividad deportiva exigente. La información disponible en la literatura y la experiencia pueden ayudar a definir cuál va a ser el tratamiento y a seleccionar apropiadamente a los pacientes que responderán bien a una intervención quirúrgica (Márquez-Arabia, 2009). En el pasado se trató conservadoramente a los pacientes con trauma de los tejidos blandos de la rodilla, pero ya se acepta, que las lesiones del LCA incrementan el riesgo de que la rodilla desarrolle osteoartritis prematura, y que su tratamiento adecuado es de suma importancia para el deportista que aspira a seguir compitiendo en el mismo nivel (López-Vidriero, 2010).
La reconstrucción artroscópica de LCA ha demostrado en el tiempo mejores resultados que el tratamiento conservador y es casi de rutina en deportistas de alto rendimiento. En la última década un mejor conocimiento de la biomecánica de la rodilla, un desarrollo importante en tecnología e instrumental y nuevas formas de rehabilitación han permitido a los deportistas de alto rendimiento volver a su práctica deportiva con mayor rapidez y a igual nivel de rendimiento que presentaban al momento de su lesión (Carrascal-Barrero, 2009).
Así, hay varios factores que influyen en estos resultados como el avance experimentado en el conocimiento de las características biomecánicas de la rodilla y los elementos de fijación del injerto, cada vez más estables y seguros en el tiempo (Radice, 2008).
Las proteínas son las responsables directas del estado y destino celulares en las distintas situaciones patológicas o traumatológicas (Anitua, 2000). Dentro de este contexto biológico están los factores de crecimiento, que controlan la evolución de los procesos de regeneración y reparación de los distintos tejidos. Los factores de crecimiento tienen capacidad para regular funciones celulares importantes como son la proliferación, migración y diferenciación celular y la síntesis de matriz extracelular. Todos estos procesos son esenciales en la reparación y regeneración. Estudios recientes in vivo e in vitro han mostrado aumentos significativos en parámetros indicadores de la actividad celular, así como mejoría de la regeneración mediante la aplicación de diversos factores de crecimiento. También, derivado de estos trabajos de investigación, se sabe que la expresión de los factores de crecimiento y de sus receptores se encuentra modulada después de una lesión y las células de los tejidos en proceso de regeneración son sensibles a la interacción con los factores de crecimiento (Sánchez, 2003a).
Así, el objetivo de este trabajo es describir nuevas estrategias de aplicación de PRGF en la cirugía artroscópica, averiguar los mecanismos moleculares que controlan la señalización celular y conducen a la regeneración de los tejidos conjuntivos: cartílago, hueso y tejidos conjuntivos blandos.
Anatomía y biomecánica del Ligamento Cruzado Anterior
Los resultados de la reconstrucción quirúrgica del LCA han mejorado con el conocimiento detallado de su estructura y función. Los conceptos anatómicos y biomecánicos importantes del LCA normal son los siguientes. Cada fibra tiene un punto único de origen e inserción, las fibras no son paralelas ni tienen la misma longitud y las fibras no están bajo la misma tensión en ningún punto del movimiento.
Las dimensiones del LCA son las siguientes: 25–38 mm de longitud, 7–12 mm de anchura y 4–7 mm de grosor. El ligamento es más angosto en la porción proximal cerca del origen femoral y se ensancha cuando alcanza la inserción tibial.
En cuanto a su microestructura, el LCA está compuesto de fibras de colágeno de 150–250 nanómetros de diámetro que se entrelazan para formar una red compleja. Varias de estas fibras se unen para formar unidades subfasciculares de 100–250 micrómetros de diámetro, cada una de ellas rodeada por una banda delgada de tejido conectivo laxo, el endotenon. Los subfascículos se unen para formar fascículos, rodeados por el epitenon. El ligamento está luego rodeado por el paratenon y la vaina sinovial. El LCA contiene estructuras neurales fusiformes consistentes en un solo axón rodeado por una cápsula fibrosa similar al órgano tendinoso de Golgi.
La irrigación del LCA proviene de las arterias genicular media (ramas ligamentosas y terminales) y geniculares inferior y lateral (ramas terminales); también del plexo sinovial.
En lo que a la biomecánica se refiere, el LCA es la primera restricción para el desplazamiento anterior de la tibia. Junto con el ligamento cruzado posterior (LCP), el LCA determina la combinación de deslizamiento y rodamiento entre la tibia y el fémur que caracteriza la cinemática de la rodilla normal. Por lo tanto, la deficiencia del LCA no solo produce episodios de inestabilidad sino también una alteración de la mecánica articular.
Cuando hay una lesión del LCA la tibia se puede subluxar anteriormente, con los signos clínicos correspondientes, pero también puede haber cambios sutiles de la función articular, por ejemplo en los desplazamientos en la localización del centro de rotación instantáneo. Se producen así fuerzas compresivas a través de la articulación que pueden explicar la enfermedad articular degenerativa acelerada que frecuentemente acompaña las lesiones de este ligamento (Márquez-Arabia, 2009).
Factores de crecimiento
En 1989, Gibble y Niss describen que el plasma concentrado de plaquetas combinado con fibrina y calcio es capaz de formar rápidamente un gel viscoso rico en plaquetas, que mejora la incorporación de tejidos e implantes en cirugía máxilo facial. Esto abrió la puerta para investigar la presencia de factores de crecimiento que se encuentran en su gran mayoría en las plaquetas del organismo.
Los factores de crecimiento son grupo de moléculas proteicas que no solo estimulan el crecimiento, sino que poseen otras acciones importantes como mantener la sobrevivencia celular, iniciar la mitogénesis y estimular la migración de las células. También producen cambios en los fenotipos que influyen en la invasión celular o la apoptosis. El concentrado plaquetario contiene una enorme cantidad de factores de crecimiento derivados de las plaquetas activadas. Estos factores están involucrados en la mayoría de los procesos biológicos de remodelación de nuestro organismo (Radice, 2008).
Tabla 1. Listado de propiedades del PRGF (López-Vidriero, 2010)
Todas las preparaciones de PRGF tienen ciertos pasos en común. El mecanismo básico para la preparación de PRGF implica extracción de sangre periférica del paciente (Figura 1, A), seguido de una centrifugación para obtener una concentración de plaquetas y citocinas por encima del valor inicial del suero (Figura 1B). El producto se centrifuga, estratificándose en tres capas en el envase. En la base se encuentra la capa roja, que está formada por eritrocitos. En el medio, una capa de color blanco que contiene leucocitos y citocinas inflamatorias y, en la parte superior, una capa amarilla que contiene plasma, plaquetas y factores de crecimiento. Se selecciona la capa amarilla que es la que más tarde se inyectará en la región seleccionada (Figura 2C).
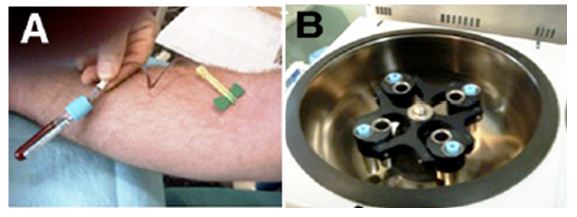
Figura 1. Extracción de sangre (A) y centrifugación de la sangre (B) (López-Vidriero, 2010).

Figura 2. Estratificado de la sangre una vez centrifugada (López-Vidriero, 2010)
Método
Se ha realizado un trabajo de revisión bibliográfica consultando en las siguientes bases de datos: Google académico, EFDdeportes.com, Scielo y Scirus, con las siguientes palabras clave: ligamento cruzado anterior, tratamiento, factores de crecimiento. No se ha acotado los años de las publicaciones de los artículos y se ha utilizado la estrategia de bola de nieve de los artículos encontrados con las palabras clave mencionados anteriormente.
Resultados
En la búsqueda bibliográfica hemos encontrado los siguientes resultados con la utilización de plasma autólogo rico en factores de crecimiento (Sánchez, 2003b):
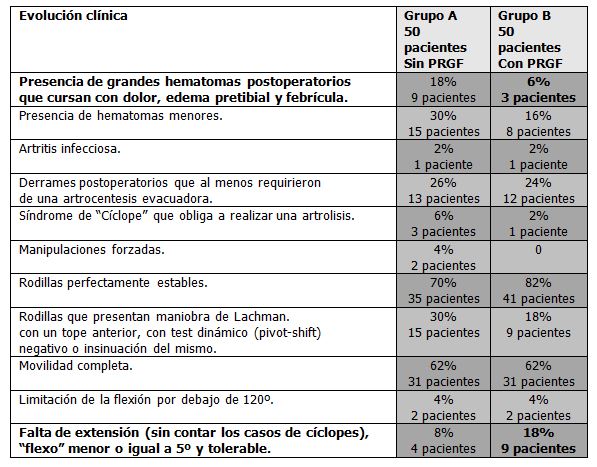
A continuación se exponen imágenes en la que podemos observar diferencias en la recuperación post lesional.
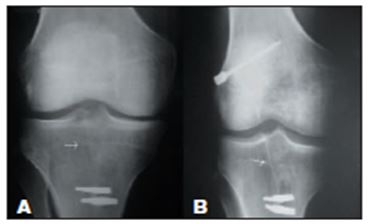
Figura 3. Radiografías postoperatorias, al mes de una intervención. Se observa la diferente
integración de los túneles tibiales (flechas). A) Con PRGF; B) Sin PRGF (Sánchez, 2003)
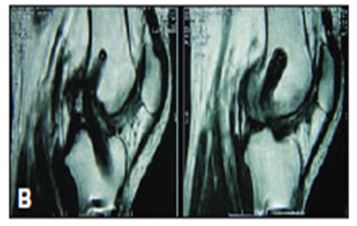
Figura 4. A) Aspecto artroscópico de la plastia del ligamento cruzado anterior tetrafascicular de
“pata de ganso”, tratado con PRGF, después de ocho meses. B) Aspecto con RM (Sánchez, 2003).
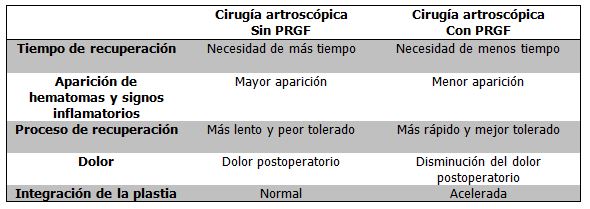
Tabla 3. Tabla resumen de las ventajas observadas en las intervenciones
realizadas con plasma autólogo rico en factores de crecimiento (Elaboración propia).
Discusión y conclusiones
Para el Deportista de Alto Rendimiento (ARD), sufrir una ruptura del ligamento cruzado anterior de su rodilla es sin duda un evento traumático y clave en su vida deportiva. La recuperación de esta lesión debe ser lo más cercana a lo normal para no afectar su rendimiento deportivo futuro y en el menor tiempo posible (Radice, 2008).
Durante los últimos años, en el área de la traumatología, se ha puesto un énfasis especial en los aspectos mecánicos. En la actualidad, se reconoce que el entorno mecánico tiene una gran influencia en la regeneración de los tejidos músculo-esqueléticos, pero no se puede ignorar el entorno biológico y los aspectos celulares. Las bases racionales para el tratamiento de lesiones traumatológicas dependerán, por tanto, de la interacción de los elementos biológicos con el entorno mecánico y de la optimización de ambos (Sánchez, 2003a).
Gracias al desarrollo de técnicas más anatómicas de reconstrucción, elementos de fijación más firmes y estables en el tiempo, protocolos de rehabilitación acelerado y equipos quirúrgicos técnicamente mejor preparados y competentes hemos tenido grandes avances en la reconstrucción quirúrgica del LCA (Radice, 2008).
Dentro de este contexto, en los últimos tiempos han aparecido múltiples trabajos dedicados al estudio y a la utilización clínica de los factores de crecimiento. Mientras se avanza en este sentido, la utilización clínica de los factores de crecimiento plaquetarios es una alternativa eficaz. La aplicación de PRGF intraarticular va a provocar, por tanto, la proliferación de las células locales de los tejidos conjuntivos densos, facilitando la reparación, y la incorporación más rápida y mejor del deportista (Anitua, 2006).
Los datos clínicos indican que la utilización de PRGF favorece la minimización de hematomas y de signos inflamatorios en el período postoperatorio. El proceso de recuperación es mejor tolerado, ya que disminuye el dolor, y además es más rápido. También parece que se acelera la integración de la plastia (Sánchez, 2003b).
Se cree también importante señalar que para autorizar el reintegro deportivo sin restricciones, se requiere que el deportista recupere íntegramente su atrofia muscular, no tenga desbalance entre extensores y flexores de su rodilla y alcance una adecuada condición física (Radice, 2008).
Las futuras vías de desarrollo incluyen la mejora de los resultados de los procedimientos artroscópicos y de la cirugía relacionada con la reconstrucción, en particular, la reconstrucción primaria del LCA. Nuevas investigaciones que tienen también como objetivo definirla dosis correcta, el tiempo y la cuantificación, así como las técnicas de aplicación ideal de PRGF (Anitua, 2006; Sánchez, 2007).
No obstante cabe decir que aún se necesitan más estudios para consensuar su utilidad.
Referencias bibliográficas
-
Anitua E., Andía I. Un nuevo enfoque en la regeneración ósea. Ed. Eduardo Anitua, Puesta al Día publicaciones, 2000.
-
Anitua E., Sánchez M., Nurden AT, et al. Autologous fibrin matrices: A potential source of biological mediators that modulate tendon cell activities. J. Biomed Mater Res A 2006; 77:285-293.
-
Carrascal-Barrero C. Lesiones en futbol: rotura de ligamento cruzado anterior. Protocolo de readaptación. EFDeportes.com, Revista Digital. Buenos Aires, Año 14, Nº 136. Sept. 2009. http://www.efdeportes.com/efd136/lesiones-en-futbol-rotura-de-ligamento-cruzado-anterior.htm
-
López-Vidriero E, et al. El uso del plasma rico en plaquetas en artroscopia y medicina deportiva: La optimización del entorno de recuperación, 2010.
-
Márquez Arabia JJ, Márquez Arabia WH. Lesiones del ligamento cruzado anterior de la rodilla. Iatreria, 2009, 22(3).
-
Radice F. Preparación del injerto de reconstrucción de ligamento cruzado anterior aplicando factores de crecimiento obtenidos de concentrado plaquetario. Videoteca, 2005. www.socht.cl.
-
Radice, F; Yáñez, R; Gutiérrez V; Pinedo, M.: Aplicación de factores de crecimiento obtenidos de concentrado plaquetario en la reconstrucción de LCA. Consejos prácticos para cuantificar su dosis y evitar su pérdida al pasar por los túneles óseos. NotiSlard 2007, 2: 7-8.
-
Radice, F, Yánez, R, Gutiérrez, V, et al. Uso de concentrado autólogo rico en factores de crecimiento en la reconstrucción del ligamento cruzado anterior. Rev. Argent Artrosc 2008; 14: S20 (Suppl 1).
-
Sánchez M., Anitua E., Azofra J., Andia I., Padilla S., Mujika I. Enhanced Achilles tendon healing with autologous plasma rich in growth factors. Br J Sports Med, 2003.
-
Sánchez M, Azofra J, Aizpurúa B, Elorriaga R, Anitua E, Andía I. Aplicación de plasma autólogo rico en factores de crecimiento en cirugía artroscópica. Cuadernos de Artroscopia 2003, 10 (19).
-
Sánchez M., Anitua E., Azofra J., Andia I., Padilla S., Mujika I. Comparison of surgically repaired Achilles tendon tears using platelet- rich fibrin matrices. Am. J Sports Med 2007; 35:245-251.
 |

Búsqueda personalizada
|
|---|---|
|
EFDeportes.com, Revista
Digital · Año 18 · N° 179 | Buenos Aires,
Abril de 2013 |
|