
|
|||
|---|---|---|---|
|
|
Adaptações moleculares das fibras musculares induzidas pelo exercício sistematizado Adaptaciones moleculares de las fibras musculares inducidas por el ejercicio sistemático Molecular adaptations of muscle fibers induced by systematic exercise |
|
|
|
*Mestre em Biologia Celular e Estrutural. Professor da Faculdade de Educação Física da Universidade Federal de Goiás, UFG **Doutor em Biologia Funcional e Molecular, Departamento de Bioquímica, Instituto de Biologia, Universidade Estadual de Campinas, UNICAMP (Brasil) |
Alexandre Donizete Ferreira* Joaquim Maria Ferreira Antunes Neto** |
|
|
|
Resumo Os músculos esqueléticos em geral são constituídos por vários tipos de fibras que expressam diferentes isoformas de miosina (MHC). As miosinas dos tipos I, IIa, IId/x e IIb estão presentes nas fibras puras dos tipos I, IIA, IID/X e IIB, respectivamente. Entre as fibras puras existem as fibras híbridas, que podem expressar duas ou mais isoformas de miosina. O objetivo deste trabalho é apresentar eventos adaptativos induzidos pelo exercício sistematizado, os quais podem conduzir a transições entre os tipos de fibras, sobretudo por alterações gênicas na expressão da miosina. Unitermos: Fibras musculares. Miosina. Adaptação. Exercício físico.
Abstract In general, the skeletal muscles are formed to several muscle fiber types that are able to express different kinds of myosin heavy chain (MHC) isoforms. The MHCI, IIa, IId and IIb will establish the pure muscle fibers of the type I, IIA, IID and IIB, respectively and, among them there are the hybrid fibers that can express two or more MHC types. The aim of this paper is to present adaptive events induced by exercise systematized, which may lead to transitions between fiber types, specially by changes in gene expression of myosin. Uniterms: Muscle fibers. Myosin. Adaptation. Physical exercise.
|
|||
|
|
EFDeportes.com, Revista Digital. Buenos Aires, Año 17, Nº 167, Abril de 2012. http://www.efdeportes.com/ |
|
|
1 / 1
Introdução
Os mecanismos de adaptação biológica são vistos como processos que possibilitam “(...) uma reorganização orgânica e funcional do organismo frente a exigências internas e externas (...) dirigida à melhor realização das sobrecargas que induz” (Weineck, 1999, p. 22). Obedecendo ao agente estressor, o funcionamento do mecanismo homeostático pode mudar e os sistemas biológicos estimulados entrarem em um novo estado funcional (Alter, 1996). Porém, fatores relevantes como a intensidade, duração e freqüência da atividade desenvolvida, além da especificidade mecânica do movimento, podem alterar o rumo de um processo adaptativo que favoreça a aquisição de padrões “rentáveis” aos mecanismos morfofuncionais celulares, gerando condições inadequadas de manutenção das capacidades de controle (Antunes Neto et al., 2006). Desta forma, o objetivo desta revisão é apresentar as estruturas moleculares constituintes do tecido músculo-esquelético e processos adaptativos específicos das fibras musculares em decorrência do exercício sistematizado.
Estrutura do tecido músculo-esquelético
O tecido músculo-esquelético é constituído por dois componentes: tecido conjuntivo, que delimita a área das estruturas protéicas do músculo, e estruturas contráteis, arranjadas em fibras, miofibrilas e miofilamentos. A organização das estruturas conjuntivas e contráteis delimita a condição morfológica e a capacidade funcional do tecido músculo-esquelético (Fleck; Kramer, 1997).
A porção de tecido conjuntivo que reveste a fibra muscular é o endomísio, contendo capilares e fibras nervosas responsáveis pelo suprimento das fibras musculares. Sob e preso ao endomísio, tem-se o sarcolema, que é a membrana da célula delimitante da unidade funcional do músculo (sarcômero). Tal como a membrana plasmática, o sarcolema permite transporte seletivo pela membrana, este que é uma propriedade essencial de membranas excitáveis. O agrupamento dos feixes musculares ou fascículos que formam as fibras musculares se dá por uma estrutura conjuntiva designada de perimísio, atuante como um separador entre as fibras, permitindo que vasos sangüíneos, vasos linfáticos e nervos tenham condições de se estenderem ao longo do músculo. O epimísio é a estrutura conjuntiva densa que envolve todos os feixes musculares, ou seja, todo o músculo (Abernethy et al., 1997). A Figura 1 apresenta as microestruturas constituintes do tecido muscular.
Como já mencionado, o aparato contrátil do tecido músculo-esquelético é formado pelas fibras, miofibrilas e miofilamentos. As fibras musculares contêm diversos núcleos, possuindo forma cilíndrica e com extremidades que se tornam delgadas progressivamente. A espessura varia de acordo com o grupo muscular ou até no mesmo músculo, podendo abranger de 10 mm a 100 mm. Em relação ao comprimento, pode-se estender da origem à inserção de um músculo. Existem diferentes tipos de fibras que podem ser delineados de acordo com suas propriedades histoquímicas, bioquímicas, morfológicas e fisiológicas. Baseando-se no tempo ao qual as fibras levam para alcançar o pico de tensão, o que também se relaciona com o tempo de relaxamento, identifica-se dois tipos principais de fibras: as fibras que possuem um tempo para pico de tensão relativamente logo, denominadas fibras de contração lenta, e as fibras com um curto tempo para atingir o pico de tensão, classificadas como fibras de contração rápida.
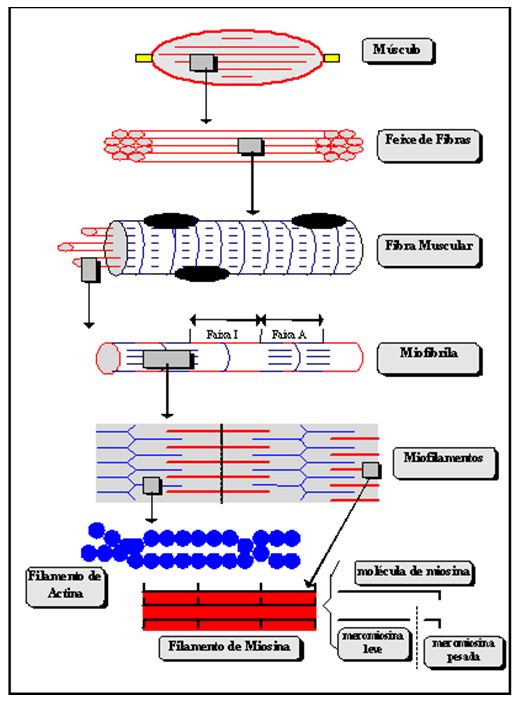
Figura 1. Estruturas moleculares do tecido músculo-esquelético (Antunes Neto, 1998)
O que parece delimitar a condição de velocidade contrátil da fibra muscular é a atividade da enzima ATPase miofibrilar da miosina; assim, fibras de contração lenta têm baixa atividade da ATPase miofibrilar, enquanto que fibras de contração rápida possuem alta atividade da ATPase miofibrilar (Bottinelli; Reggiani, 2000; Parcel et al., 2003; Williamson et al., 2001). As fibras de contração rápida podem ser subdivididas em tipo IIa, IIb e IIc, dependendo da conteúdo de ATPase miofibrilar identificado histoquimicamente em pH de baixa amplitude. As fibras dos tipos IIa e IIb têm propriedades cinéticas similares, porém com padrões transitórios distintos quanto às propriedades da miosina. As características das fibras tipo IIc não são tão conhecidas em relação às demais. Discute-se que as fibras tipo IIc podem ser uma fibra intermediária que permite a transformação de fibras tipo IIa e IIb em fibras tipo I (Goldspink, 2003). Quanto às características metabólicas, as fibras tipo I não possuem um sistema enzimático glicolítico tão desenvolvido como o das fibras tipo II. Elas são ricas no conteúdo mitocondrial e de mioglobina - com alto potencial para o metabolismo aeróbio - e a densidade da rede capilar é mais desenvolvida ao redor das fibras quando comparadas com as fibras do tipo II. Já as fibras do tipo II detêm uma atividade da miosina ATPase elevada, com um sistema enzimático glicolítico muito bem desenvolvido, atividade oxidativa e conteúdo mitocondrial baixos e um condicionamento elevado para fadiga (Schiaffino; Reggiani, 1994; Pette; Staron, 1997; Staron et al., 1999).
Estudo de Staron (1997) mostra que, por delineamento de diferença da sensibilidade de pH da adenosina trifosfato miofibrilar (m-ATPase), que se correlaciona com a diferença no conteúdo da cadeia pesada da miosina, há uma heterogeneidade quanto ao padrão histoquímico e funcional dos tipos das fibras tipo I e tipo II. Sete tipos de fibras podem ser classificadas, de acordo com a capacidade da relação ativação/inativação da m-ATPase de cada fibra após pré-incubação em pH específico: I, IC, IIC, IIAC, IIA, IIAB, IIB. As fibras mais similares às fibras do tipo I (indistinguíveis das fibras do tipo I após pré-incubação ácida, mas com coloração intermediária após pré-incubação alcalina) são do tipo IC; aquelas fibras mais similares às fibras do tipo II (indistinguíveis das fibras rápidas após pré-incubação alcalina, mas com coloração intermediária após pré-incubação ácida em pH de 4.3) são do tipo IIAC. Algumas fibras permanecem com coloração oculta através das amplitudes do pH (pH 10.4, pH 4.3 e pH 4.6), sendo denominadas de fibras do tipo IIC. A Tabela 1 apresenta a classificação mais difundida das fibras do tecido músculo-esquelético e suas características metabólicas:
Tabela 1. Classificação das fibras musculares de acordo com eventos bioquímicos. Adaptado de Fleck, Kramer (1997)
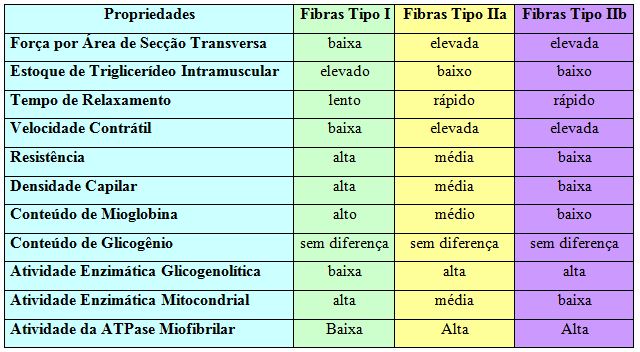
Como visto, o sistema músculo-esquelético é uma formação heterogênea de vários tipos de fibras musculares. A quantificação de diferentes tipagens bioquímicas das fibras musculares tem proporcionado o desenvolvimento de vários sistemas de classificação. Apesar da similaridade classificatória, há diferenças marcantes (Tabela 2).
Tabela 2. Sistema de classificação das fibras musculares. Adaptado de Fleck e Kramer (1997)
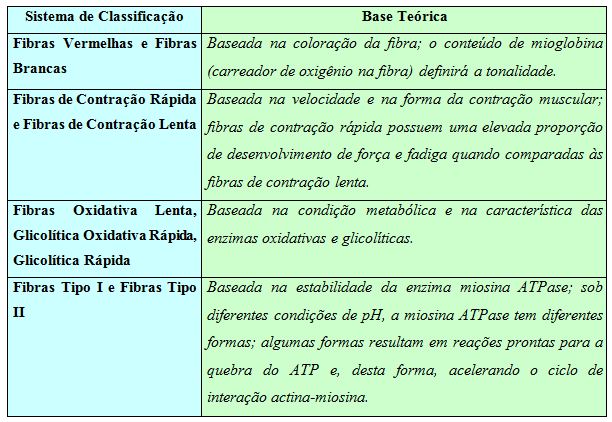
As miofibrilas compõem a fibra muscular, sendo arranjadas em paralelo umas às outras, possuindo diâmetro de 1 a 3 mm. Através de análises microscópicas, percebe-se que as miofibrilas são constituídas por estruturas protéicas, com áreas claras e escuras alternadas: a justaposição das áreas claras e escuras é que confere ao tecido músculo-esquelético o padrão estriado. As áreas ou faixas claras são designadas faixas isotrópicas I, enquanto que as escuras recebem a denominação de faixas anisotrópicas A. Esta classificação é decorrente da velocidade de uma onda luminosa ao atravessar as faixas: ao atravessar a faixa I, a velocidade da luz emergente é a mesma em todas as direções (isotrópica), de forma que a faixa anisotrópica (faixa A) possibilita diferentes velocidades ao longo de sua extensão. No meio da faixa I há uma estria delgada e escura, classificada como disco ou linha Z. A região compreendida entre dois discos Z constitui a unidade morfológica e funcional do tecido músculo-esquelético: o sarcômero (Antunes Neto, 1998).
O sarcômero é formado por proteínas contráteis diferenciadas, que são os miofilamentos. As faixas I e A são constituídas por dois tipos de miofilamentos: os miofilamentos espessos, que se localizam na parte média do sarcômero, e os miofilamentos finos, ligados aos discos Z. Tanto a actina quanto a miosina são dotadas de diversos tipos protéicos. Os miofilamentos finos são preponderantemente dotados de actina, contudo possuindo também proteínas regulatórias (tropomiosina e troponina). Cada filamento de actina é composto por dois cordões helicoidais de F-actina (fibrosa), proteína essa resultante de um polímero de moléculas de G-actina (globular). Em ligação com a G-actina tem-se a tropomiosina (duas correntes espiralizadas com 284 aminoácidos cada uma), cuja função é impedir a ativação da actina pelo cálcio. Há também o complexo troponina, composto por três subunidades: a troponina-T, que liga troponina a tropomiosina, a troponina-I, inibidora de quatro a sete moléculas de G-actina de ligação à miosina quando a tropomiosina está presente, e a troponina-C, que pode reversivelmente ligar íons cálcio em função da concentração deste. A miosina, proteína formadora do miofilamento espesso, é composta por duas cadeias longas que terminam em duas cabeças globulares. A molécula da miosina pode ser decomposta em fragmentos de meromiosina leve e meromiosina pesada, sendo a meromiosina pesada subdividida em subfragmentos 1 e 2. As cabeças globulares (uma contém ATP e a outra um sítio de ligação a actina) são chamadas de S1, enquanto que a porção restante da meromiosina pesada é dita S2. Ainda em relação aos miofilamentos, existem mais duas estruturas protéicas com função de organização do sarcômero: a nebulina, um filamento inextensível que acompanha a actina, e a titina (ou conectina), proteína elástica filamentosa importante na configuração e manutenção geométrica da miosina (Antunes Neto, 1998; Louboutin et al., 1996). A Figura 2 apresenta uma ilustração esquemática do sarcômero.
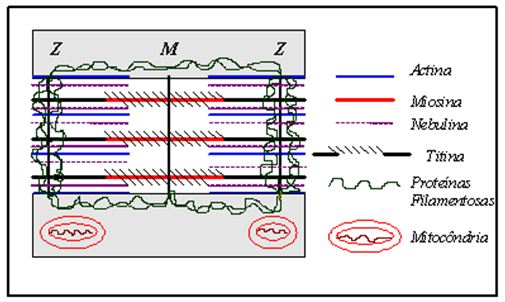
Figura 2. Estruturas moleculares do sarcômero. Adaptado de Waterman-Storer (1991) e Antunes Neto (1998)
Fibras musculares, estrutura da miosina e exercício sistematizado
Como já abordado, a miosina pode ser clivada em dois fragmentos, a miosina de cadeia leve (myosin light chain, MLC) que constitui o eixo da molécula e a miosina de cadeia pesada (myosin heavy chain, MHC), compreendendo o segmento mais curto, globular e dotado de atividade ATPasica (Vemuri et al., 1999; Wahrmann et al., 2001). A MHC é a estrutura protéica que entrará em contato com o sítio ativo da actina através da degradação de moléculas de ATP, permitindo o deslizamento da actina sobre a miosina e conseqüente encurtamento das fibras musculares, culminado na contração (Talmadge; Roy, 1993; Bigard et al., 1996). As miosinas de cadeia pesada são formadas por isoformas de proteínas que vão hidrolisar o ATP em velocidades diferentes, permitindo que as fibras possam ser classificadas em dois grupos, um de contração lenta e outro de contração rápida (Fleck; Kramer, 1997).
As fibras de contração lenta expressam MHCI, enquanto as MHCIIa, IId/x e IIb estão presentes nas fibras de contração rápida (Schiaffino; Reggiani, 1994; Pette; Staron, 1997; Staron et al., 1999). Em roedores encontram-se as isoformas de miosina I, IIa, IId/x e IIb, já em humanos são encontradas as miosinas I, IIa e IIb. Atualmente, as isoformas IIb de humanos tendem a ser classificadas como IId/x, pelo fato, dessas apresentarem velocidade de contração semelhante à dos roedores (Bottinelli; Reggiani, 2000; Parcel et al., 2003; Williamson et al., 2001). E também, alguns pesquisadores têm identificado a presença do gene MHCIIb no genoma humano, no entanto a evidência da expressão dessa proteína na prática não tem sido significativa (Goldspink, 2003; Weiss et al., 1999). As fibras que expressam essas isoformas são ditas puras do tipo I, IIA, IID/X e IIB. Entre as fibras puras, encontram se aquelas que são formadas por duas ou mais isoformas de miosina em proporções diferentes (IC = MHCI > MHCIIa, IIC = MHCIIa = MHCI, IIAC= MHCIIa > MHCI, IIAD = MHCIIa > MHCIId, IIDB = MHCIId > MHCIIb), sendo classificadas como fibras híbridas (Di Maso et al., 2000; Pette; Staron, 2000). Assim, pode-se delinear no mínimo 10 tipos diferentes de fibras musculares em ratos: I, IC, IIC, IIAC, IIA, IIAD, IIDA, IID, IIDB e IIB (Pette; Staron, 2000), e em humanos é possível obter 7 tipos: I, IC, IIC, IIAC, IIA, IIAB, IIB (Fry, 2004; Pette; Staron, 2000, Pette; Staron, 1993).
Essa diversidade de fibras torna os músculos estriados esqueléticos capazes de responder a diversos estímulos, levando a alterações moleculares que têm início no interior da célula, através da expressão de genes específicos que regulam a produção dos diferentes tipos de miosina (Goldispink, 2003). Tais genes permitirão, por sua vez, a transcrição de novas moléculas de RNAm e conseqüente tradução de proteínas específicas (Willoughby; Pelsue, 2000), indo culminar na expressão do fenótipo adaptado. Os estímulos podem tanto ter um caráter endógeno quanto exógeno. Entre os estímulos endógenos pode-se citar alterações na atividade neuromuscular, alterações nos níveis hormonais e idade. Nos exógenos encontram-se aqueles fatores que agem sobre o organismo através de influências externas: estimulação elétrica, carga mecânica, ausência de carga, microgravidade e exercício físico (Roy et al., 1997; Jakubiec-Puka et al., 1999; Mannion, 1999).
Um dos fatores externos de grande importância na alteração do comportamento das fibras musculares é o exercício físico (Goldspink, 1998; Williamson et al., 2000; Pette, Staron, 2001; Williamson et al., 2001; Parcell et al., 2003), que permitirá transição das fibras tanto no sentido de lento para rápido (I=>IIA=>IID=>IIB) quanto de rápido para lento (IIB=>IID=>IIA=>I), sendo que essa mudança não se dá sempre para os extremos, mas para aquelas fibras que melhor respondem metabolicamente ao estímulo aplicado. Essas transições se dão através da modulação da intensidade e duração do treinamento (Bompa; Cornacchia, 1998; Andersen et al., 2000). A aplicação de um treinamento físico de baixa intensidade e longa duração pode induzir uma conversão de fibras rápidas em fibras lentas, por outro lado, um treinamento de alta intensidade e curta duração pode causar um resultado oposto, isto é, conversão de fibras lentas para rápidas (Caiozzo et al., 2000; Campos et al., 2002).
As respostas adaptativas ao treinamento são resultados de convergências entre fatores intrínsecos aos exercícios executados e as condições endógenas/exógenas interferentes na qualidade de vida do sujeito (Figura 3). Rietveld (1996) sugere que os organismos são controlados homeostaticamente, com uma série de fatores que se manifestam para permitir uma adaptação ótima às condições do meio. O treinamento físico busca, por meio de estratégias metodológicas fundamentadas no conhecimento científico, a aplicação de um conjunto de estímulos que desequilibrem a homeostasia do sistema morfofuncional do organismo e, desta forma, providencie um estímulo para a adaptação. O desequilíbrio em homeostasia requererá do organismo a reorganização de seu mecanismo funcional para o restabelecimento de um estado homeostático ideal: a adaptação positiva será o resultado de uma alternância corretamente programada entre indução de estresse e regeneração. Assim, o organismo adapta-se ao agente estressor tanto que, se um mesmo estímulo for imposto novamente após a ocorrência da adaptação, os mecanismos homeostáticos não serão rompidos na mesma extensão (Fry et al., 1992).
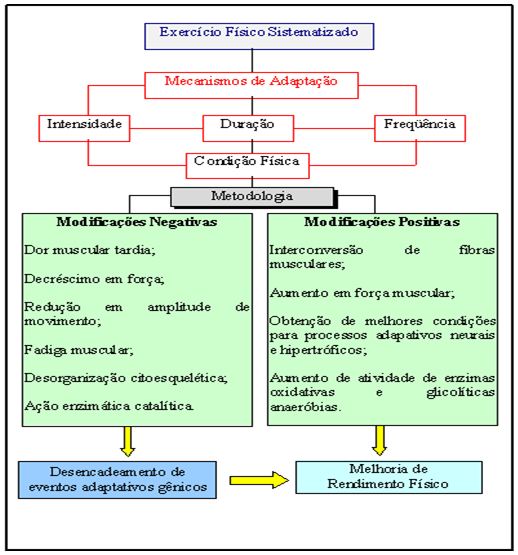
Figura 3. Correlação dos eventos adaptativos orgânicos e moleculares ao exercício físico. Adaptado de Antunes Neto (1998)
Estudos têm sugerido que treinamento intervalado em sprint pode induzir uma transição bidirecional em direção às fibras do tipo IIA por uma conversão das isoformas presentes nas fibras I e IIB (Luginbuhl et al., 1984; Esbjörnsson et al, 1993), proporcionando um melhor aproveitamento da energia, pois a quantidade de ATP produzido por uma fibra do tipo IIA é maior do que o da fibra do tipo IIB, resultando assim numa melhora da performance. Isto leva a acreditar que o treinamento aplicado pode ter induzido mudanças nos níveis de MHC dentro das fibras do músculo semitendinoso através de perturbações nos genes que expressam essas proteínas (Harrison et al., 2002), promovendo transição das fibras musculares em direção àquelas que não utilizam exclusivamente a via aeróbia ou anaeróbia para obtenção de energia.
Mudanças na secção transversal das fibras musculares são percebidas durante um determinado treinamento físico, o que caracteriza um aumento na síntese das proteínas contrateis, entre elas as miosinas (Booth et al., 1998). Nesse trabalho, não houve mudanças significativas no tamanho das fibras musculares da região vermelha. Já na região branca houve um expressivo aumento da área das fibras IIB e no músculo inteiro pode ser visto uma hipertrofia nas fibras IIBD, ambas representantes do grupo de contração rápida. De acordo como estudos anteriores, as fibras mais recrutadas em exercícios de curta duração são as de contração rápida, o que poderia induzir uma alta produção das proteínas de algumas dessas fibras, causando hipertrofia das mesmas (Bottinelli and Reggiani, 2000; Talmadge, 2000; Lin et. al., 2002). Notou-se que, apesar de não significante, teve um aumento do volume da banda IIB, levantando a hipótese de que houve aumento na síntese dessa miosina.
Considerações finais
As respostas adaptativas ao exercício físico decorrem de estímulos metabólicos distintos – aeróbio e anaeróbio –, integrados entre si e ou com variáveis orgânicas múltiplas. Sabe-se também que o estresse mecânico, sobretudo advindo das contrações musculares excêntricas, pode intervir no desencadeamento tanto de respostas lesivas quanto de adaptações positivas. Os resultados dependerão do potencial de influência dos estímulos específicos sobre a estrutura alvo, o que poderá gerar regras de adaptação prevalecentes na rotina de treinamento. As fibras musculares mostraram grande plasticidade em adaptar-se a tais regras de adaptação, o que abre um amplo espectro de estudo na perspectiva da biodinâmica do movimento humano.
Referências bibliográficas
-
ABERNETHY, A. B. et al. The biophysical foundations of human movement. Champaign: Human Kinetics, 1997.
-
ALTER, M. J. Science of stretching. Champaign: Human Kinetics Books, 1996.
-
ANDERSEN, J. L. et al. Muscle, genes, and athletic performance. Sci Am., v. 283, p. 48-55, 2000.
-
ANTUNES NETO, J. M. F. et al. Circulating leukocyte heat shock protein 70(hsp70) and oxidative stress markers in rats after a bout of exhaustive exercise. Stress, v. 09, n. 02, p. 107–115, 2006.
-
ANTUNES NETO, J. M. F. Modificações morfo-funcionais do tecido muscular induzidas pela atividade excêntrica: um estudo global dos processos adaptativos. Dissertação de Mestrado. Universidade Estadual de Campinas: Faculdade de Educação Física, 1998.
-
BIGARD, X. A. et al. Endurance training affects myosin heavy chain phenotype in regenerating fast-twich muscle. J Appl Physiol., v. 81, n. 6, p. 2658-2665, 1996.
-
BOMPA, T.; CORNACCHIA L. Serious strenght training. Editora Human Kinetics. 1998.
-
BOOTH, F. W. et al. Molecular and cellular adaptation of muscle in response to physical training. Acta Physiol. Scand., v. 162, p. 343-350, 1988.
-
BOTTINELLI, R.; REGGIANI, C. Human skeletal muscle fibres: molecular and functional diversity. Prog. Biophys. Mol. Bio., v. 73, p. 195-262, 2000.
-
CAIOZZO, V. J. et al. MHC polymorphism in rodent plantaris muscle: effects of mechanical overload and hypothyroidism. Am. J. Physiol. Cell. Physiol., v. 278, p. C709-C717, 2000.
-
CAMPOS, G. E. R. et al. Muscular adaptations in response to three different resistance-training regimens: specificity of repetition maximum training zones. Eur J. Appl. Physiol., v. 88, p. 50-60, 2002.
-
DI MASO, N. A. et al. Single-fiber myosin heavy chain polymorphism during postnatal development: modulation by hypothyroidism. Am. J. Physiol. Regul. Integ. Comp. Physiol., v. 278, p. R1099-R1106, 2000.
-
ESBJÖRNSSON, M. et al. (1993) Muscle fibre type changes with sprint training: effect of training pattern. Acta Physiol. Scand., v.149, p. 45-246, 1993.
-
FLECK, S. J.; KRAEMER, W. J. Designing resistance training programs. Champaign: Human Kinetics, 1997.
-
FRY, A. The role of resistance exercise intensity on muscle fibre adaptations. Sports Med., v. 34, n. 10, p. 663-679, 2004.
-
FRY, R. W. et al. Periodisation of training stress - a review. Can. J. Sports Sci., v. 17, n. 3, p. 234-240, 1992.
-
GOLDSPINK, G. Selective gene expression during adaptation of muscle in response to different physiological demands. Comp. Biochem. Physiol., v. 120, part b, p. 5-15, 1998.
-
GOLDISPINK, G. Gene expression in muscle in response to exercise. J. Muscle Res. Cell M., v. 24, p. 121-126, 2003.
-
HARRISON, B. C., et al. Skeletal muscle adaptations in response to voluntary wheel running in myosin heavy chain null mice. J. Appl. Physiol., v. 92, p. 313-322, 2002.
-
LIN, J. Transcriptional coactivator PGC-1α drives the formation of slow-twich muscle fibres. Nature, v. 418, p. 797- 801, 2002.
-
JAKUBIEC-PUKA, A. et al. Contents of myosin heavy chains in denervated slow and fast rat leg muscles. Comp. Biochem. Physiol., v. B 122, p. 355-362, 1999.
-
LOUBOUTIN, J. P. et al. Propriétés structurales et fonctionnelles du muscle strié squelettique. Médicine du Sport, v. 70, n. 05, p. 189-195, 1996.
-
LUGINBUHL A. J. et al. Fiber type changes in rat skeletal muscle after intense interval training. Histochemistry, v. 81, p. 55-58, 1984.
-
MANNION, A. F. Fibre type characteristics and function of the human paraspinal muscles: normal values and changes in association with low back pain. J. Electromyogr. Kines. v. 9, p. 363-377, 1999.
-
PARCELL, A. C. et al. Single muscle fiber myosin heavy hain distribution in elite female track athletes. Med. Sci. Sports Exerc., v. 35, n. 3, p. 434- 438, 2003.
-
PETTE, D.; STARON, R. S. The continuum of pure and hybrid myosin heavy chain-based types in rat skeletal muscle. Histochemistry, v. 100, p. 149-153, 1993.
-
PETTE, D.; STARON, R. S. Mammalian skeletal muscle fiber type transitions. Int. Rev. Cytol., v. 170, p. 143-223, 1997.
-
PETTE, D.; STARON, R. S. Myosin isoforms, muscle fiber types, and transitions. Microsc. Res. Tech., v. 50, p. 500-509, 2000.
-
PETTE, D.; STARON, R. S. Transitions of muscle fiber phenotypic profiles. Histochem. Cell. Biol., v. 115, p. 359-372, 2001.
-
RIETVELD, W. J. General introduction to chronobiology. Br. J. Med. Biol. Research, v. 29, n. 01, p. 63-70, 1996.
-
ROY, R. R. et al. Modulation of MHC isoforms in functionally overloaded and exercised rat plantaris fibers. J. Appl. Physiol., v. 83, p. 280-290, 1997.
-
SCHIAFFINO, S.; REGGIANI, C. Myosin isoforms in mammalian skeletal muscle. J. Appl. Physiol., v. 77, n. 2, p. 493-501, 1994.
-
STARON, R. S. Human skeletal muscle fiber types: delineation, development, and distribuition. Can. J. Appl. Physiol., v. 22, n. 4, p. 307-327, 1997
-
STARON, R. S. et al. Fiber type composition of four hindlimb muscles of adult Fisher 344 rats. Histochem. Cell. Biol., v. 111, p. 117-123, 1999.
-
TALMADGE, R. J.; ROY, R. R. Eletrophoretic separation of rat skeletal muscle myosin heavy-chain isoforms. J. Appl. Physiol., v. 75, n. 5, p. 2337-2340, 1993.
-
VEMURI, R. et al. The stretch-activation response may be critical to the proper functioning of the mammalian heart. Proc. Natl. Acad. Sci. USA, v. 96, p. 1048-1053, 1999.
-
WAHRMANN, J. P. et al. Plasticity of skeletal myosin in endurance trained rats (I). A quantitative study. Eur. J. Appl. Physiol., v. 84, p. 367-372, 2001.
-
WEINECK, J. Biologia do esporte. São Paulo: Manole, 1991.
-
WEISS, A. et al. Organization of human and mouse skeletal myosin heavy chain gene clusters is highly conserved. Proc. Natl. Acad. Sci. USA, v. 96, p. 2958-2963,1999.
-
WEISS, A. et al. Comparative sequence analysis of the complete human sarcomeric myosin heavy chain family: implications for functional diversity. J. Mol. Biol., v. 290, p. 61-75, 1999.
-
WILLIAMSON, D. L. et al. Progressive resistence training reduces myosin heavy chain co-expression in single muscle fibers from older men. J. Appl. Physiol., v. 88, p. 627-633, 2000.
-
WILLIAMSON, D. L. et al. Reduction in hybrid single muscle fiber proportions with resistance training in humans. J. Appl. Physiol., v. 91, p. 1955-1961, 2001.
-
WILLOUGHBY, D. S.; PELSUE, S. Effects of high-intensity strength training on steady state myosin heavy chain isoform mRNA expression. JEPonline, v. 3, n. 4, p. 13-25, 2000.
Outros artigos em Portugués
 |

Búsqueda personalizada
|
|---|---|
|
EFDeportes.com, Revista
Digital · Año 17 · N° 167 | Buenos Aires,
Abril de 2012 |
|